El fenómeno de la radiación consiste en la propagación de energía en forma de ondas electromagnéticas o partículas subatómicas a través del vacío o de un medio material.
Para que esta radiación sea ionizante (capacidad de ionizar un átomo, separarle un electrón), deben tener suficiente energía.
En el gráfico e espectro electromagnético se observa que hay capacidad de ionización cuando las ondas electromagnéticas superan el rango de lo visible, estando en la frontera de la ionización las ondas ultravioletas pertenecientes al rango visible.
Tras estas explicaciones dadas en clase se han propuesto los siguientes ejercicios:
1) Calcular cuantos átomos hay en 1 cm da arista de un cubo del material que elijas.
Como ejemplo vamos a ver cuantos átomos hay en 1Cm3 de sal (NaCl).
La densidad de la sal es 2,16g/cm3, por lo tanto en 1cm3 tenemos 2,16 g de sal.
Primero se calcula la masa molar del material (M)
M = Nº atómico Na * 1 +Nºatómico Cl *1 = 23+35= 48 g/mol.
Para saber el número de moles (n) que tenemos en 1cm3:
n= (2,16g/cm3)/(48g/mol)= 0,045mol/cm3.
Con lo que podemos hallar en número de moléculas contenidas en esos moles (N) teniendo en cuenta en número de avogadro (6.022x10^23 moléculas/mol):
N=0,045 mol NaCl ·6,022x10^23 moléculas/mol =0,27x10^23 moléculas
Y sabiendo que cada molécula contiene dos atómos (Uno de Na y otro de Cl) tendremos los siguientes átomos en 1cm3 de sal:
Átomos en 1cm3 de sal= 2,7x10^22 · 2 =5,598x10^22 átomos en 1cm3.
2) ¿Qué foton tiene más energía uno rojo o uno azul?
El fotón es la partícula portadora de
todas las formas de radiación electromagnética.
Se
comporta como una onda en fenómenos como la refracción que
tiene lugar en una lente, o en la cancelación por interferencia destructiva de ondas
reflejadas; sin embargo, se comporta como una partícula cuando
interactúa con la materia para transferir una cantidad fija de energía, que
viene dada por la expresión:
donde h es
la constante de Planck (6,626·10^(-34)
J·s), c es la velocidad de la luz,  es
la longitud de onda y
es
la longitud de onda y  la frecuencia de la
onda.
la frecuencia de la
onda.
El foton rojo pertenece a frecuencias de 4,9·10^14 Hz (s-1)
E(foton rojo)= 6,626·10^(-34) J·s ·4,9·10^14 Hz (s-1) = 3,24x10^-19 julios
El foton azul pertenece a frecuencias de 5,8·10^14 Hz (s-1)
E(foton azul)= 6,626·10^(-34)
J·s ·5,8·10^14 Hz
(s-1) = 3,84x10^-19 julios
Para ver mejor la diferencia de energías
se halla el porcentaje de esta diferencia de energia:
%= E(foton azul)/E(foton rojo)=3,84x10^-19 julios/3,24x10^-19
julios=1,18.
Es decir un
fotón azul de longitud de oda de 580nm tendrá un 18% más de energia que un
foton rojo con 490nm.

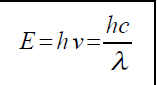
No hay comentarios:
Publicar un comentario